Introducción
En la industria farmacéutica, la validación de sistemas críticos es un requisito indispensable para garantizar la calidad de los medicamentos y la seguridad de los pacientes. Dentro de este proceso, la Calificación de Diseño (DQ) es la primera etapa formal que asegura que el sistema ha sido concebido y documentado de acuerdo con las necesidades del usuario y los requisitos regulatorios.
¿Qué significa la Calificación de Diseño
La DQ consiste en la revisión y aprobación del diseño propuesto para un sistema, equipo o instalación crítica, verificando que:
- Cumpla con las especificaciones del usuario (URS).
- Integre los requisitos de Buenas Prácticas de Manufactura (GMP).
- Considere aspectos de seguridad, calidad y trazabilidad.
- Sea técnicamente viable y cumpla con normas aplicables (ISO, FDA, EMA, COFEPRIS).
En otras palabras, la DQ asegura que el sistema “nace bien diseñado” antes de pasar a etapas de construcción, instalación y operación.
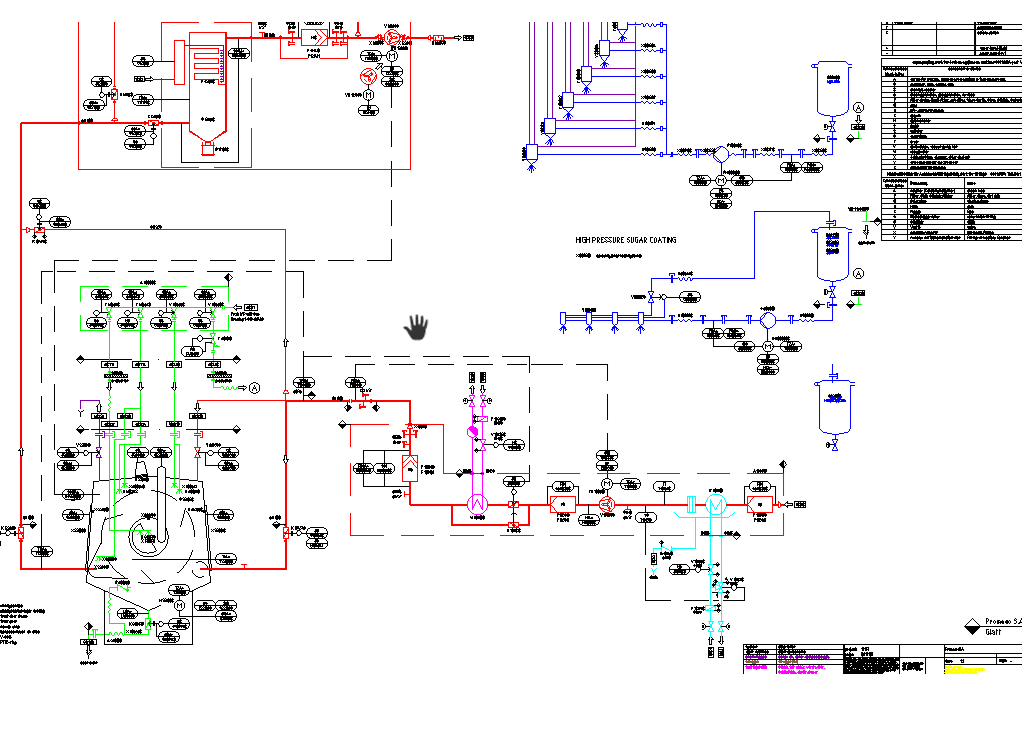
Ejemplo práctico: Sistema de agua para inyección (WFI)
Supongamos que una planta farmacéutica requiere un sistema de generación y distribución de agua para inyección (WFI).
En la DQ se revisa:
- Capacidad de producción: litros por hora requeridos según la demanda de la planta.
- Materiales de construcción: acero inoxidable grado farmacéutico (AISI 316L).
- Diseño higiénico: tuberías con pendiente adecuada, soldaduras orbitales, ausencia de puntos muertos.
- Normas aplicables: cumplimiento con USP, EP y guías de la OMS.
- Documentación técnica: planos, diagramas de flujo, especificaciones de equipos, manuales de fabricante.
Solo después de aprobar la DQ, el proyecto puede avanzar hacia la Calificación de Instalación (IQ) y etapas posteriores.
Importancia de la DQ en validación
- Previene desviaciones: asegura que el sistema cumpla desde el inicio con lo requerido.
- Reduce costos: evita modificaciones posteriores por errores de diseño.
- Facilita auditorías: proporciona evidencia documental de que el sistema fue concebido bajo estándares regulatorios.
- Protege la calidad del producto: garantiza que el sistema no comprometa la seguridad del paciente.
Conclusión
La Calificación de Diseño es el primer paso crítico en la validación de sistemas farmacéuticos. Es un proceso documental y técnico que asegura que el sistema cumple con las necesidades del usuario y las regulaciones aplicables antes de su construcción e instalación. Un ejemplo claro es el sistema de agua para inyección, donde la DQ garantiza que el diseño sea higiénico, seguro y trazable.